醫院新聞
陶勇團隊在Nature子刊發表研究成果“基于自愈合大孔微球的外泌體眼內緩釋劑型”
近日,首都醫科大學附屬北京朝陽醫院(以下簡稱朝陽醫院)眼科主任陶勇教授基于多年的慢性眼底疾病臨床診療經驗,與中國科學院過程工程研究所生化工程國家重點實驗室馬光輝院士和魏煒研究員團隊合作,提出了“類細胞”劑型的新策略,進行了玻璃體視網膜疾病治療的研究,相關工作發表于Nature Biomedical Engineering上。
近年來,細胞療法在眼科疾病治療領域獲得了越來越多的關注,并且已經在臨床試驗中顯示出獨特的療效。然而,該創新療法仍面臨著體內細胞存活率低、病理環境下細胞表型不穩定、細胞產品保存條件苛刻等一系列難題。已有研究表明,旁分泌是細胞發揮治療作用的機制之一。因此,科研人員開始思考利用更為穩定的細胞分泌成分(如外泌體)作為藥效組分,對眼部相關疾病進行治療。
首先,研究人員基于獨創的自愈合大孔微球(Cap)來負載外泌體(Exo)。由此所構建的ExoCap體系可以在尺寸、內部結構和分泌行為方面實現對功能性細胞的模擬。此外,ExoCap在玻璃體腔中向下沉降,可以避免出現活細胞注射后漂浮在玻璃體腔中影響視野的副作用;隨后,ExoCap緩慢降解,長效釋放其內裝載的活性外泌體。
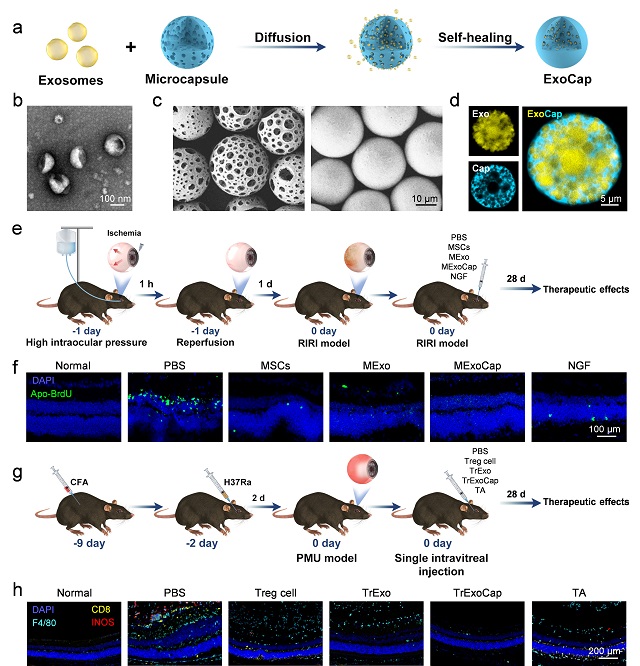
鑒于該體系構建的通用性和靈活性,可以按照不同治療需求負載不同細胞來源的外泌體。研究人員在小鼠視網膜缺血再灌注損傷(RIRI)模型中證明,大孔微球裝載間充質干細胞外泌體(MExo)可以有效地阻止視網膜細胞凋亡,效果顯著優于神經生長因子(NGF)治療方案;同時也在小鼠和食蟹猴致敏分枝桿菌性葡萄膜炎(PMU)模型中證明了,大孔微球裝載調節性T細胞外泌體(TrExo)可以抑制眼內炎癥,副作用較糖皮質激素例如曲安奈德(TA)治療方案顯著更低。
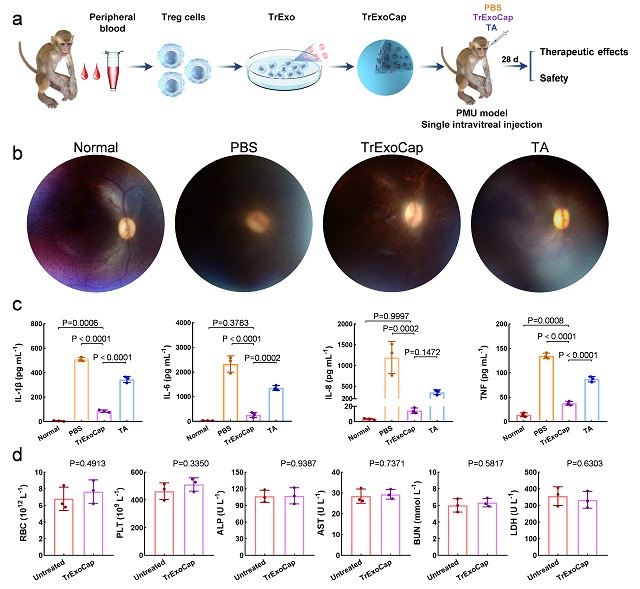
據研究人員介紹,上述成果仍屬于動物水平的臨床前研究,實際臨床療效仍有待進一步研究。鑒于ExoCap僅包含細胞外泌體組分和FDA批準的PLGA材料,并且在小鼠和食蟹猴模型中顯示了較好的安全性和有效性,該創新劑型具有較大的臨床轉化潛力。研究團隊正在按照相關要求合作推進臨床個體化治療的研究。
本工作是陶勇團隊基于以往的研究基礎,在眼底病治療領域的新突破。包晗碩士及田穎博士為該論文共同第一作者,陶勇教授(朝陽醫院)、魏煒研究員(過程工程研究所)和馬光輝院士(過程工程研究所)為共同通訊作者。該工作得到了國家自然科學基金項目、北京自然科學基金項目、北京順義區科技成果轉化協調服務平臺建設基金、北京市醫院管理中心“登峰”人才培養計劃的支持。
下一篇: 泌尿外科舉辦中德腎移植學術研討會







 京公網安備11010502033042
京公網安備11010502033042